I. Visão geral doESMODiretrizes de 2025
Em agosto de 2025, a ESMO lançou oficialmente o guia de prática clínica para diagnóstico, tratamento e acompanhamento do câncer de pulmão de não pequenas células em estágios iniciais e localmente avançados, publicado no renomado periódico de oncologia Annals of Oncology. Esta é a primeira atualização abrangente desde a versão de 2017 e oferece uma referência extremamente confiável para oncologistas do mundo todo.

O câncer de pulmão apresenta a maior incidência e mortalidade entre todas as neoplasias malignas no mundo. A cada ano, são registrados mais de 2,2 milhões de novos casos e mais de 1,8 milhão de óbitos, tornando o câncer de pulmão a principal causa de morte relacionada ao câncer em homens e mulheres. O câncer de pulmão de não pequenas células (CPNPC) representa aproximadamente 80-85% de todos os casos de câncer de pulmão. Diante desse cenário preocupante, a publicação da diretriz de 2025 injeta um novo ímpeto científico na prática clínica, sendo a atualização das estratégias de testes de biomarcadores particularmente crucial.
II. Interpretação das principais atualizações das diretrizes
2.1 Testes de Biomarcadores: De “Opcional” a “Essencial”
A diretriz de 2025 representa um marco no ajuste estratégico em relação aos testes de biomarcadores. A diretriz afirma explicitamente que os testes de biomarcadores são essenciais para a tomada de decisão terapêutica em pacientes com câncer de pulmão de não pequenas células (CPNPC) em estágios IB a III.
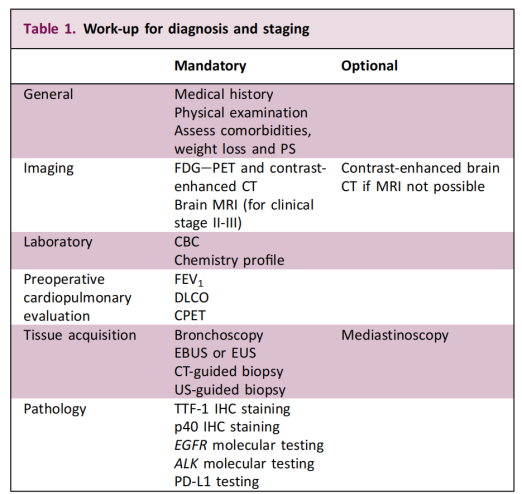
Esta recomendação amplia o escopo dos testes moleculares, que antes se concentravam em pacientes com doença avançada, para incluir também casos em estágio inicial e ressecáveis. O objetivo principal é identificar mutações genéticas causadoras da doença e fornecer uma base científica para o tratamento personalizado e de precisão. A diretriz também enfatiza que a viabilidade da biópsia e a abordagem diagnóstica devem ser determinadas por uma equipe multidisciplinar, com base nas características do paciente e do tumor.
Em relação à estratégia específica de testes, a diretriz recomenda claramente que os testes genéticos sejam realizados antes da tomada de decisão cirúrgica e que abranjam, no mínimo, EGFR e ALK. Esse conceito de "testagem prévia" tem profunda importância clínica para a estratificação precisa e o tratamento personalizado do câncer de pulmão de não pequenas células (CPNPC) em estágio inicial – a rapidez e a precisão dos resultados dos testes determinam diretamente a escolha da terapia adjuvante subsequente.
2.2 Avanços terapêuticos no câncer de pulmão de não pequenas células (CPNPC) em estágio inicial com oncogenes condutores positivos
A diretriz de 2025 integra evidências de múltiplos estudos clínicos importantes para estabelecer um caminho claro de tratamento de precisão para pacientes com câncer de pulmão de não pequenas células (CPNPC) em estágio inicial com oncogenes condutores positivos.
Pacientes com mutação positiva no EGFR:Com base no estudo ADAURA, um marco na área, o osimertinibe adjuvante pós-operatório por três anos tornou-se o padrão global de tratamento para pacientes com deleções no éxon 19 do EGFR ou mutações L858R no éxon 21. O estudo ADAURA é um estudo internacional, multicêntrico, randomizado e controlado de fase III que avaliou a eficácia e a segurança do osimertinibe adjuvante em pacientes com câncer de pulmão de não pequenas células (CPNPC) com mutação no EGFR, em estágios IB-IIIA, completamente ressecados. O estudo demonstrou que o osimertinibe melhorou significativamente tanto a sobrevida livre de doença quanto a sobrevida global em comparação com o placebo, estabelecendo o osimertinibe como o novo padrão de tratamento para essa população. No entanto, análises exploratórias do estudo ADAURA indicaram que aproximadamente 36% das descontinuações precoces do tratamento foram motivadas por eventos adversos e outros 31% por decisão do paciente. Essa constatação destaca a necessidade de testes basais precisos antes do tratamento para garantir que a terapia direcionada seja administrada aos pacientes que podem obter benefício sustentado.
Pacientes ALK-positivos:Com base no estudo ALINA, o tratamento adjuvante pós-operatório com alectinibe por dois anos tornou-se o padrão de tratamento. Na análise primária do estudo ALINA, um ensaio clínico randomizado de fase III aberto, o alectinibe demonstrou um benefício significativo na sobrevida livre de doença (SLD) na população com CPNPC em estágios II-IIIA, com uma razão de risco (HR) de 0,24. Dados atualizados do estudo ALINA, apresentados no congresso ESMO 2025, mostraram que, após ≥3 anos de acompanhamento, o benefício em SLD com alectinibe permaneceu “sustentado e clinicamente significativo”, com uma HR de 0,36 na população com CPNPC em estágios II-IIIA. A taxa de sobrevida global (SG) em 4 anos relatada mais recentemente atingiu 98,4%, a taxa de SLD em 4 anos foi de 75,5% e a SLD no sistema nervoso central também apresentou melhora, sem novos sinais de alerta de segurança. Esses dados robustos consolidam ainda mais o alectinibe adjuvante como o padrão de tratamento após a ressecção de CPNPC ALK-positivo e reforçam a importância de testes precisos para identificar esses pacientes.
Escolha do método de teste:A diretriz da ESMO de 2025 lista explicitamenteEnsaios de painel de RT-PCR multiplexJuntamente com NGS baseado em RNA, IHC e FISH, como uma das abordagens técnicas recomendadas para a detecção da fusão ALK. Isso indica que o requisito fundamental da diretriz é realizar testes para orientar as decisões clínicas, em vez de impor uma plataforma de teste específica. Para produtos de RT-PCR focados na detecção de EGFR e ALK, essa estratégia de teste flexível fornece uma forte justificativa baseada em diretrizes para seu uso na prática clínica.
III. Soluções Técnicas para Testes de Precisão
A diretriz de 2025 antecipa os testes para a fase de tomada de decisão pré-cirúrgica, elevando o padrão de precisão, sensibilidade e acessibilidade dos ensaios. Os dois produtos de detecção baseados em RT-PCR descritos abaixo estão em perfeita consonância com os requisitos da diretriz do ponto de vista técnico.
3.1 Kit de Detecção de Mutação EGFR – Plataforma de Tecnologia ARMS Aprimorada
Tecnologia centralA tecnologia ARMS aprimorada permite a amplificação específica de sequências mutantes de baixa abundância em um fundo de alta abundância de tipo selvagem.
Três salvaguardas técnicas:
-ARMS aprimorado → melhora o reconhecimento de mutações
-Enriquecimento enzimático → digere a sequência de fundo do tipo selvagem e enriquece as sequências mutantes.
-Bloqueio por temperatura → suprime a amplificação não específica
DesempenhoSensibilidade deFrequência do alelo mutante de 1%
Controle de contaminaçãoControle interno integrado + enzima UNG previne contaminação
Tempo de respostaOperação em tubo fechado, aproximadamente120 minutos
Compatibilidade de amostras:Tecido/biópsia líquidaamostras → aborda o requisito de “testes prévios”
Cobertura:45 mutaçõesnos exons 18-21 do EGFR, correspondendo precisamente às regiões destacadas pelas diretrizes (deleções no exon 19 e L858R no exon 21)
Uso clínico: Orienta diretamente a terapia com EGFR-TKI
Kit de Detecção de Fusão 3.2 MMT EML4-ALK – Solução de Detecção de Fusão Baseada em RNA

-Plataforma tecnológicaRT-PCR baseado em RNA – oferece vantagens inerentes sobre os métodos baseados em DNA para detecção de fusões.
-Vantagem baseada em RNADetecta diretamente transcrições de fusão expressas, evitando efetivamente falsos negativos.
-Evidências do estudoEm fusões ALK de baixa abundância, o RT-PCR é significativamente mais confiável do que os testes baseados em DNA.
-SensibilidadeDetecta fusões até20 cópias por reação
-Cobertura de variantes: Capas12 variantes comuns de fusão EML4-ALK(incluindo a variante 1 ~33%; variantes 3a/3b juntas ~29%)
-Operação e controle de contaminação: Tubo fechado, ~120 minutos; controles de processo integrados + enzima UNG previnem resultados falsos
-Compatibilidade do instrumentoCompatível com diversos instrumentos de PCR em tempo real convencionais.
-Alinhamento de diretrizesAltamente consistente com as diretrizes da ESMO.
IV. Consistência entre os ensaios e as recomendações das diretrizes
Os dois produtos de detecção são altamente consistentes com a diretriz ESMO 2025 para câncer de pulmão de não pequenas células em estágios iniciais e localmente avançados, nas seguintes dimensões principais:
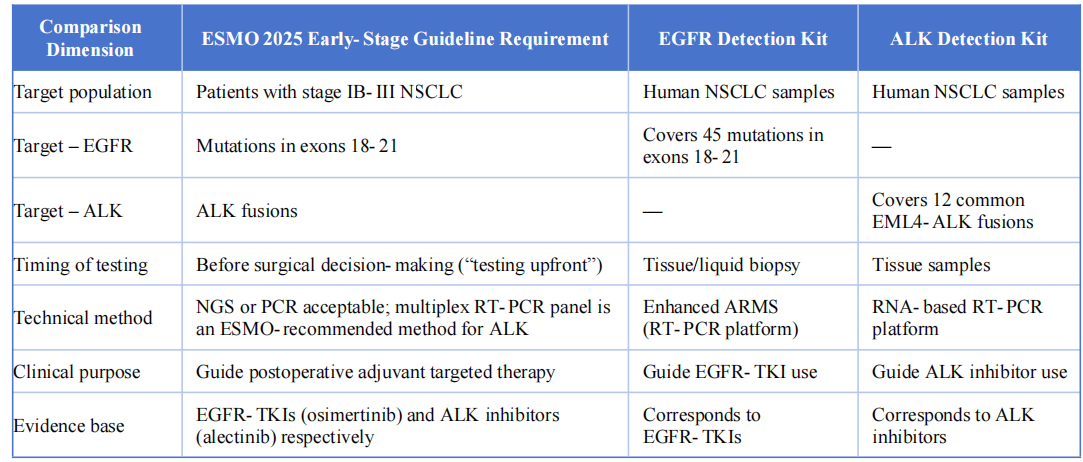
V. Conclusão
A diretriz ESMO 2025 para CPNPC em estágio inicial inaugura uma nova era de diagnóstico e tratamento de precisão, centrada em “Testes prévios, direcionamento preciso e otimização do tratamento.Os kits de detecção de mutação EGFR e de fusão MMT EML4-ALK atendem aos requisitos das diretrizes em relação a alvos, tempo e precisão por meio de caminhos técnicos distintos.
O kit EGFR utiliza tecnologia ARMS aprimorada para detecção de alta sensibilidade de mutações específicas em amostras limitadas, suportando tanto biópsia tecidual quanto líquida para possibilitar o "teste prévio".
O kit ALK é baseado em RT-PCR de RNA, oferecendo vantagens sobre os métodos de DNA para detecção de fusões, estando em consonância com a recomendação da ESMO de painéis de RT-PCR multiplex para testes de ALK.
Em conjunto, estes dois produtos formam uma solução de testes de precisão em conformidade com as diretrizes da ESMO 2025, apoiando a terapia adjuvante personalizada para o câncer de pulmão de não pequenas células (CPNPC) em estágio inicial.
Referências:
- Zer A, Ahn MJ, Barlesi F, et al. Câncer de pulmão de células não pequenas em estágios iniciais e localmente avançados: Diretriz de Prática Clínica da ESMO para diagnóstico, tratamento e acompanhamento. Ann Oncol. 2025;36(11):1245-1262. doi:10.1016/j.annonc.2025.08.003
Data da publicação: 06/05/2026

