O dia 24 de março de 2026 marca o 31º Dia Mundial da Tuberculose. A Organização Mundial da Saúde (OMS) anunciou o tema global deste ano como:“Sim! Podemos acabar com a tuberculose!”, enfatizando que uma forte liderança governamental, um compromisso político sustentado e uma ação multissetorial coordenada são essenciais para acabar com a epidemia de tuberculose (TB).

Progresso global e desafios remanescentes
De acordo com o Relatório Global sobre Tuberculose de 2025, o controle global da tuberculose alcançou um marco significativo em 2024, com ambos os grupos alcançando uma redução significativa na taxa de mortalidade e no número de casos de tuberculose.incidência e mortalidade em declíniopela primeira vez desde a pandemia de COVID-19.
Uma estimativa10,7 milhões de pessoasEm 2024, 54% dos casos de tuberculose ocorreram em homens, 35% em mulheres e 11% em crianças e adolescentes. Dentre esses casos, aproximadamente619.000 (5,8%)estavam coinfectados com o HIV, e390.000 (3,6%)eram tuberculose multirresistente ou resistente à rifampicina (TB-MDR/RR).
A tuberculose causou aproximadamente1,23 milhão de mortesem 2024, permanecendo a principal causa infecciosa de morte em todo o mundo, ultrapassando a COVID-19. Após três anos de aumentos entre 2021 e 2023, a incidência global de TB diminuiu em quase 2% em 2024, refletindo uma recuperação gradual dos serviços de TB.[1]
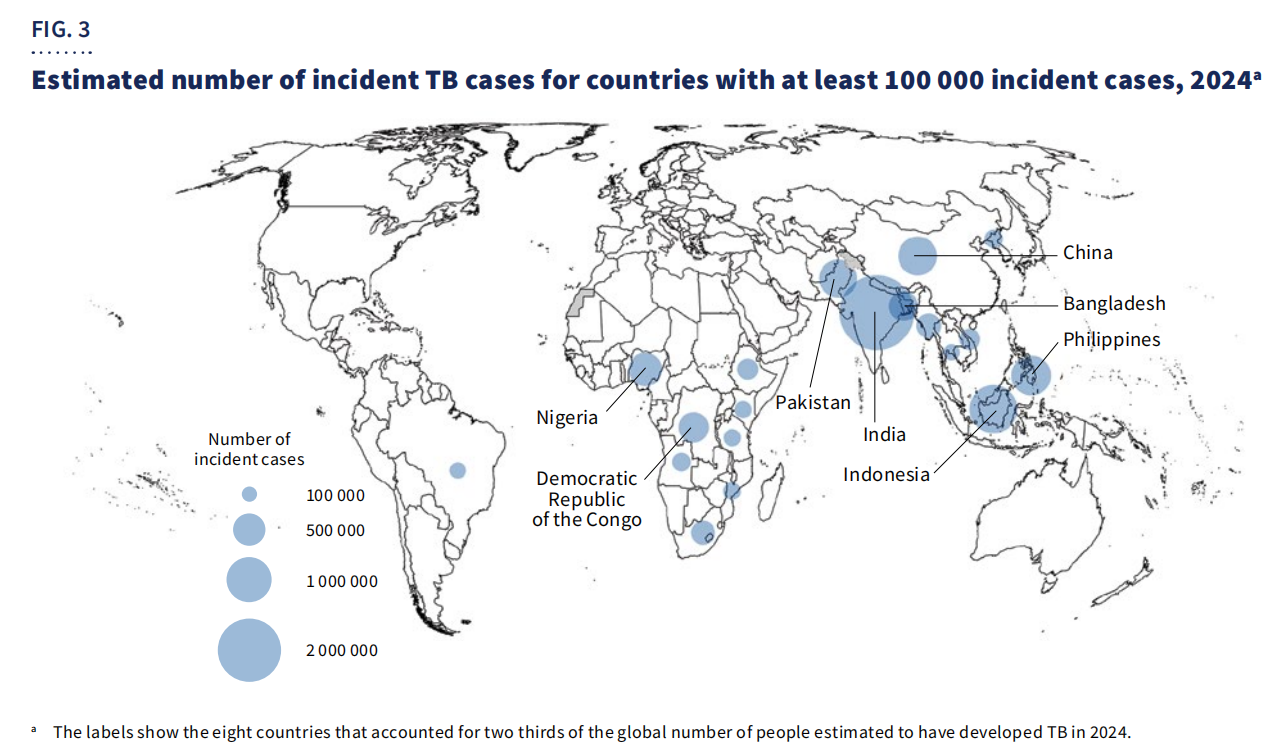
Geograficamente,67% dos casosestavam concentradas em oito países: Índia, Indonésia, Filipinas, China, Paquistão, Nigéria, República Democrática do Congo e Bangladesh.
Apesar dos progressos, a tuberculose continua sendo uma das principais causas de morte entre pessoas vivendo com HIV e um importante fator de mortalidade associado à resistência antimicrobiana. O financiamento global continua insuficiente, com apenasUS$ 5,9 bilhõesdisponível em 2024—muito abaixo doMeta anual de US$ 22 bilhõesPrevisto para 2027.
Esses números destacam a necessidade urgente de fortalecer os programas de controle da tuberculose em todo o mundo, com foco na ampliação do acesso ao diagnóstico, na melhoria dos resultados do tratamento e no enfrentamento dos determinantes sociais que impulsionam a transmissão da doença. A tuberculose continua a exigir uma sólida cooperação internacional e um compromisso político para atingir as metas da Estratégia para o Fim da Tuberculose.
Mycobacterium tuberculosis: Patogênese e Classificação
Mycobacterium tuberculosis (MTB/M. tuberculosis) é o patógeno primário e mais comum responsável pela tuberculose (TB). Ele pode entrar no corpo humano através do trato respiratório, trato digestivo ou pele e membranas mucosas danificadas, infectando múltiplos órgãos e causando diferentes formas de TB. A TB pulmonar, transmitida principalmente por gotículas, representa mais de 80% dos casos de TB. Os sintomas comuns incluem tosse, produção de escarro e hemoptise. Após a infecção nos pulmões, a bactéria pode se disseminar pela corrente sanguínea para múltiplos sistemas, podendo levar à TB óssea, urinária ou gastrointestinal.[2]
O MTB faz parte do gênero Mycobacterium, que inclui:
- Complexo Mycobacterium tuberculosis (MTBC): Compreende M. tuberculosis, M. bovis, M. africanum, M. canettii e M. microti, entre outros. Embora M. tuberculosis seja a principal causa da tuberculose, M. bovis e M. africanum também podem induzir a doença.
- Micobactérias não tuberculosas (MNT).
- Mycobacterium leprae, a bactéria causadora da hanseníase.
Abordagens de diagnóstico laboratorial
O diagnóstico preciso e oportuno é essencial para o controle eficaz da tuberculose. A Organização Mundial da Saúde enfatiza queAs tecnologias de diagnóstico molecular rápido transformaram fundamentalmente a detecção da tuberculose, permitindo a identificação altamente sensível e específica de patógenos, além da detecção simultânea da resistência a medicamentos.[1].
- Microscopia e Culturae: A cultura continua sendo o padrão ouro para o diagnóstico da tuberculose, pois permite a identificação definitiva de organismos viáveis e auxilia nos testes de sensibilidade a medicamentos e na análise genômica. No entanto, devido à lenta taxa de crescimento do Mycobacterium tuberculosis, os resultados geralmente levam de 2 a 8 semanas, o que limita sua utilidade clínica em tomadas de decisão urgentes.
-Testes imunológicos: Os métodos imunológicos, incluindo o teste cutâneo de tuberculina (TST) e os ensaios de liberação de interferon-gama (IGRA), detectam as respostas imunes do hospedeiro à infecção por tuberculose. Embora úteis para identificar infecção latente, esses ensaios não conseguem distinguir de forma confiável entre infecção ativa e pregressa e, portanto, têm especificidade diagnóstica limitada em contextos de alta incidência.
-Diagnóstico Molecular (NAAT): Testes baseados em DNA, como a amplificação de ácidos nucleicos (NAAT), são recomendados devido à sua alta sensibilidade e especificidade.
-Sequenciamento de nova geração direcionado (tNGS): As tecnologias de sequenciamento direcionado proporcionam identificação de alta resolução de mutações associadas à resistência. As diretrizes da OMS recomendam o tNGS como uma ferramenta avançada para a detecção de resistência a medicamentos após o diagnóstico, apoiando estratégias de tratamento de precisão [3].
-Sequenciamento metagenômico de próxima geração (mNGS): O sequenciamento metagenômico permite a detecção imparcial de uma ampla gama de patógenos sem a necessidade de seleção prévia do alvo. Essa abordagem é particularmente valiosa em cenários clínicos complexos ou pouco claros, incluindo infecções mistas e pacientes imunocomprometidos, nos quais os diagnósticos convencionais podem ser insuficientes.
A OMS destaca ainda que a confirmação microbiológica é essencial para iniciar a terapia adequada e melhorar os resultados dos pacientes, reforçando a importância da integração de diagnósticos moleculares avançados nos programas de controle da TB [1].
Soluções completas de diagnóstico molecular da Macro & Micro-Test
1.Detecção por PCR multiplex para tuberculose e resistência a medicamentos.TB
| Código do produto | Nome do produto | Certificação |
| HWTS-RT001 | Kit de detecção de DNA de Mycobacterium tuberculosis (PCR por fluorescência) | CE |
| HWTS-RT137 | Kit de detecção de mutação de resistência à isoniazida em Mycobacterium tuberculosis (curva de fusão) | CE |
| HWTS-RT074 | Kit de detecção de ácido nucleico e resistência à rifampicina do Mycobacterium tuberculosis (curva de fusão) | CE |
| HWTS-RT102 | Kit de detecção de ácido nucleico baseado na amplificação isotérmica por sonda enzimática (EPIA) para Mycobacterium tuberculosis | CE |
| HWTS-RT144 | Kit de detecção de ácido nucleico do complexo Mycobacterium tuberculosis liofilizado (amplificação isotérmica com sonda enzimática) | CE |
| HWTS-RT105 | Kit de detecção de DNA de Mycobacterium tuberculosis liofilizado (PCR por fluorescência) | CE |
| HWTS-RT147 | Kit de detecção de ácido nucleico de Mycobacterium tuberculosis e resistência à rifampicina e isoniazida (curva de fusão) | CE |
Quando há forte suspeita clínica de tuberculose (TB),HWTS-RT147O teste é recomendado para a detecção qualitativa da infecção por MTB e da tuberculose multirresistente (TB-MDR). Este teste identifica mutações no gene da MTB.gene rpoB, que levam à resistência à rifampicina (RIF) e mutações nogenes katG e InhA, que estão associadas à resistência à isoniazida (INH). Oferece um teste eficiente, realizado em uma única sessão, para MTB e TB multirresistente (TB-MDR), incorporando controle de qualidade interno para minimizar resultados falso-negativos, garantindo resultados rápidos e precisos.
2.Sequenciamento direcionado PTNseq para patógenos respiratórios e perfil de resistência
| Código do produto | Nome do produto | Especificação. |
| HWKF-TS0001 | Kit de enriquecimento de genes de patógenos para infecção da corrente sanguínea PTNseq | 24 testes/kit |
| HWKF-TS0002 | Kit de Enriquecimento de Genes de Microorganismos Patogênicos para Infecção do Sistema Nervoso Central PTNseq | 24 testes/kit |
| HWKF-TS0003 | Kit de enriquecimento de genes de patógenos de infecção respiratória PTNseq | 24 testes/kit |
| HWKF-AT0003 | Kit de construção de biblioteca de enriquecimento automatizado de microrganismos patogênicos para infecção respiratória PTNseq (ONT) | 24 testes/kit |
| HWKF-TS0004 | Kit de enriquecimento genético para patógenos infecciosos de amplo espectro PTNseq | 24 testes/kit |
| HWKF-TS0005 | Kit de enriquecimento genético de microrganismos patogênicos infecciosos de amplo espectro PTNseq | 24 testes/kit |
| HWKF-TS0151 | Kit para tipagem de micobactérias e enriquecimento de genes de resistência a medicamentos (método de amplificação múltipla) | 24 testes/kit |
Em casos de infecções respiratórias mistas (incluindo infecções do trato respiratório superior e inferior, tuberculose e doenças respiratórias crônicas), ou quando a análise de genes de resistência a medicamentos é necessária (por exemplo, suspeita de tuberculose resistente a medicamentos), oSérie PTNseq de detecção gênica direcionada de alto rendimentoPode ser aplicado. Baseado em tecnologia avançada de sequenciamento direcionado, o PTNseq emprega PCR ultramultiplex para enriquecer sequências-alvo específicas, combinada com sequenciamento de alto rendimento e tecnologia de nanoporos de terceira geração para identificação abrangente de patógenos e perfil de resistência a medicamentos.
O sistema utiliza primers patenteados de alta especificidade para a amplificação ultramultiplex de genes-alvo. Com o suporte de um banco de dados proprietário e algoritmos bioinformáticos inteligentes, ele proporciona a identificação precisa de patógenos, juntamente com a análise de genes de resistência a medicamentos e de virulência. O enriquecimento direcionado reduz a interferência do DNA do hospedeiro, melhorando a sensibilidade em amostras com alto teor de DNA humano e permitindo a detecção eficaz de alvos complexos, como...Mycobacterium tuberculosis, fungos, bactérias intracelulares, vírus de RNA e genes de resistência ou virulência.
PTNseq atinge um limite de detecçãotão baixo quanto 100 cópias/mLe cobre175 patógenos respiratórios comuns, incluindo 76 bactérias, 73 vírus, 19 fungos, 7 micoplasmas, bem comoClamídia, Rickettsiae 54 genes de resistência a medicamentosO painel inclui oMycobacterium tuberculosismicobactérias não tuberculosas complexas e importantes.
A série PTNseq combina alta sensibilidade com custo-benefício, melhorando as taxas de detecção de patógenos e apoiando a terapia antimicrobiana individualizada, além de ajudar a mitigar a resistência antimicrobiana. Integrada ao sistema totalmente automatizado de preparação de bibliotecas de sequenciamento genético (AIOS), ela oferece uma solução hospitalar simplificada com um tempo de resposta de apenas 6,5 horas, da amostra ao resultado.

3. Sequenciamento metagenômico para detecção de patógenos de amplo espectro
| Código do produto | Nome do produto | Especificação. |
| HWKF-MN0011 | Kit de Detecção Metagenômica de Patógenos (DNA-Illumina) | 24 testes/kit |
| HWKF-MN0018 | Kit de Detecção Metagenômica de Patógenos (DNA-MGI) | 24 testes/kit |
| HWKF-MN0021 | Kit de Detecção de Patógenos Metagenômicos (DNA-ONT) | 24 testes/kit |
| HWKF-MN0012 | Kit de Detecção Metagenômica de Patógenos (RNA-Illumina) | 24 testes/kit |
| HWKF-MN0019 | Kit de Detecção Metagenômica de Patógenos (RNA-MGI) | 24 testes/kit |
| HWKF-MN0022 | Kit de Detecção de Patógenos Metagenômicos (RNA-ONT) | 24 testes/kit |
| HWKF-MN0013 | Kit de Detecção Metagenômica de Patógenos (DNA+RNA-Illumina) | 24 testes/kit |
| HWKF-AYM0013 | Kit de construção automatizada de biblioteca para detecção de patógenos metagenômicos (DNA+RNA-Illumina) | 24 testes/kit |
| HWKF-MN0020 | Kit de Detecção Metagenômica de Patógenos (DNA+RNA-MGI) | 24 testes/kit |
| HWKF-MN0023 | Kit de Detecção Metagenômica de Patógenos (DNA+RNA-ONT) | 24 testes/kit |
Quando o diagnóstico clínico não for claro,detecção de genes de patógenos por mNGS de alto rendimentoPode ser realizado em diversas amostras do paciente, incluindo fluido de lavagem broncoalveolar, escarro, swabs de garganta, sangue, derrame pleural, pus e amostras de tecido. Essa abordagem utiliza a tecnologia de sequenciamento metagenômico, na qual diferentes amostras passam por um pré-tratamento direcionado, seguido de extração de ácido nucleico utilizando esferas de vidro e enzimas digestoras de parede celular, aumentando a eficiência da extração. O sequenciamento é adaptado a múltiplas plataformas, garantindo um alto volume de dados para melhorar a sensibilidade do mNGS e a integridade da montagem. Os dados são analisados utilizando um banco de dados desenvolvido internamente e algoritmos inteligentes para detecção.mais de 20.000 patógenos, incluindo bactérias, fungos, vírus e parasitas, fornecendo informações sobre microrganismos suspeitos de serem patogênicos. Este método é adequado para pacientes de difícil diagnóstico, em estado crítico ou imunocomprometidos, incluindo a identificação deMTBcomplexoeNTM, bem como infecções mistas. Melhora significativamente as taxas de detecção de patógenos e ajuda a orientar o uso clínico direcionado de antibióticos, permitindo um diagnóstico preciso da infecção.
Conclusão
Embora progressos substanciais tenham sido alcançados, a tuberculose continua sendo um grande desafio global para a saúde, particularmente no contexto da resistência a medicamentos, da falta de financiamento e do acesso desigual ao diagnóstico.
A OMS enfatiza que ampliar o acesso a diagnósticos moleculares rápidos e tecnologias avançadas de sequenciamento é essencial para alcançar os objetivos da Estratégia para o Fim da Tuberculose. Com inovação contínua, investimento e colaboração global, acabar com a tuberculose não é mais uma aspiração, mas um objetivo alcançável.
Referências:
- Organização Mundial da Saúde. Relatório Global sobre Tuberculose 2024/2025: Testes de Diagnóstico e Tratamento.
- Organização Mundial da Saúde. Manual da OMS para a seleção de testes moleculares de diagnóstico rápido recomendados pela OMS para a detecção de tuberculose e tuberculose resistente a medicamentos.
- Organização Mundial da Saúde. Diretrizes consolidadas da OMS sobre tuberculose: Módulo 3 – Diagnóstico (atualização de 2024).
Data da publicação: 24/03/2026
